Evènement thromboembolique veineuse (ETV) sévères révélatrices d’une COVID-19 à propos d’une observation
Mamadou DIAKITE1, Bourema DEMBELE1, Jean Paul DEMBELE2, Yacouba CISSOKO2, Samba SIDIBE1, Mariam SAKO1, Alou SANGARE1, Souleymane COULIBALY1, Sounkalo DAO2.
1 : Service de Cardiologie CHU Point ‘’G’’, Bamako, Mali, 2 : Service de Maladie Infectieuse et Tropicale CHU Point ‘’G’’ Bamako, Mali.
L’infection à ‘’Severe acute respiratory syndrome coronavirus 2’’ (SARS-CoV-2) est une maladie complexe à plusieurs visages, qui fait intervenir des phases : virale, inflammatoire et thrombotique. Nous rapportons une présentation foudroyante (détresse respiratoire) d’évènements thrombo-emboliques veineuses chez le sujet jeune féminin en surpoids et sous contraception oestroprogestative. Cliniquement c’est un tableau d’insuffisance respiratoire aigu avec des signes de lutte respiratoire. Les explorations complémentaires trouvent un syndrome inflammatoire biologique, une élévation des D-dimères à plus de neuf fois la normale. Une embolie pulmonaire (EP) massive proximale et bilatérale associée à des lésions parenchymateuses en verre dépoli à l’angio-tomodensitométrie pulmonaire et une thrombose subtotale de la veine fémorale commune à la veine poplité gauche avec présence de deux thrombi flottants dans la fémorale profonde à l’ultra sonographie doppler des membres. Le diagnostic de l’infection par le SRAS-CoV2 a été posé sur la base de la sérologie. Mise sous oxygène et traitement l’évolution a été favorable. Les ETEV sont de primun movens au cours de la COVID-19 ; c’est aussi un challenge diagnostic et de prise en charge car nécessite une équipe multidisciplinaire.
Severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) is a complex disease with many faces, which involves: viral phase, inflammatory phase and thrombotic phase. We report an overwhelming presentation (respiratory failure) of venous thromboembolic events in overweight young female subjects on progesteron contraception. Clinically it is a picture of acute respiratory failure with signs of respiratory struggle. Further investigations find a biological inflammatory syndrome, an elevation of D-dimer to more than nine times normal. A proximal and bilateral massive pulmonary embolism associated with parenchymal lesions in ground glass with Computed tomography pulmonary angiography and a subtotal thrombosis of the femoral vein common to the left popliteal vein with the presence of two floating thrombi in the deep femoral by Compression ultrasonography from upper-limb. The diagnosis of SRAS-CoV2 was done on serology. Putting on oxygen and treatment, the evolution was favorable. VTE (venous thrombo-embolism) are a primary concern during COVID-19; it is also a diagnostic and management challenge because it requires a multidisciplinary team.
Mamadou Diakité, Cardiologue, service de cardiologie, Centre-Hospitalier Universitaire-Point ‘’G’’. Téléphone : (+223) 74196750 - (+223) 60007400, Email : diakitemamadoua@yahoo.fr
Introduction
L’infection à « Severe acute respiratory syndrome coronavirus 2 » (SARS-CoV-2) ou COVID-19, est une maladie complexe à plusieurs visages, qui fait intervenir des phases : virale, inflammatoire et thrombotique [1]. Bien que le tableau respiratoire causé soit au premier plan ; des manifestations extra-pulmonaires ont été observées, notamment au niveau du système vasculaire [2]. En effet, une incidence anormalement élevée d’événements thromboemboliques veineux (ETEV) a été observé, en particulier chez les patients souffrant des formes les plus sévères et hospitalisés en réanimation [3]. De plus, leur survenue au cours de la COVID-19 aggrave le pronostic des patients [4]. Nous rapportons chez le sujet jeune une forme clinique inhabituelle à révélation foudroyante sur le système cardio-respiratoire.
Observation :
HD âgée de 39 ans, multi geste avec trois enfants vivants et un décédé, patiente sous contraceptif oestroprogestatif depuis deux ans. Elle a subitement présenté nuitamment une détresse respiratoire, pour laquelle elle nous consulte en urgence. Poids= 102 Kg, Taille=178 cm ; indice de masse corporelle (IMC)= 31,6 Kg/m2 tours de taille (TT)= 107cm. L’examen clinique trouve : une patiente anxieuse, polypnéique à 32 cycles par minute, avec signes de lutte respiratoire, un pouls à 115 bpm, une TA : 160/120 mm Hg, une température à 37°8C et une saturation en oxygène du sang périphérique (SapO2) à 80% à l’air ambiant qui passe sous oxygène haute concentration 12 litres/min à 88%. Les conjonctives sont normo-colorées. L’examen physique retrouve à l’auscultation cardio-pulmonaire, des bruits du cœur rapides et assourdis sans bruits sur ajoutés et des poumons libres de râles. Par ailleurs on note une absence de signes d’insuffisance cardiaque périphériques et le signe de Homans est négatif.
Au total : Syndrome d’insuffisance respiratoire aigüe avec fébricule chez une jeune dame obèse sous COP.
Devant ce tableau nous avons pensé à un cœur pulmonaire aigue dont l’étiologie pourrait être une embolie pulmonaire (EP) vu le score de probabilité clinique pré test développé aux urgences (trie des patients aux urgences) et les D-dimères.
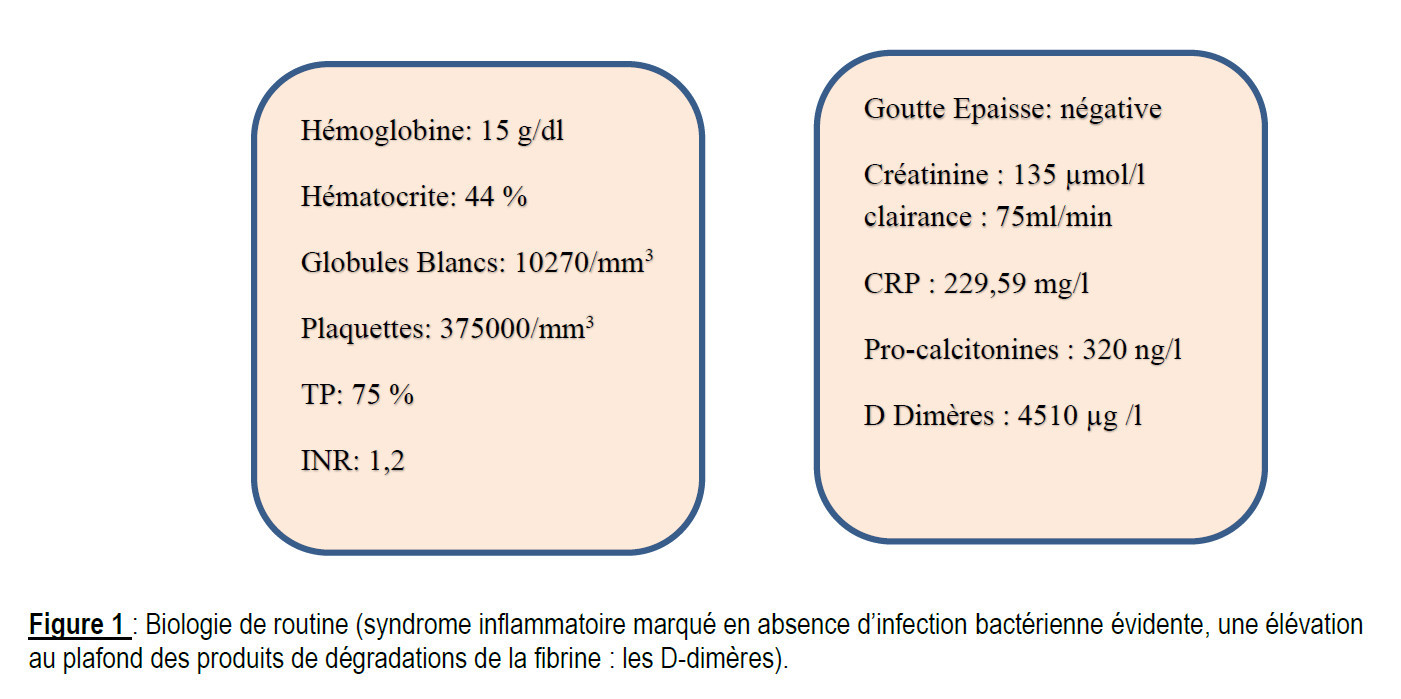
Parallèlement à ce raisonnement clinique le bilan recommandé en urgence (si accessible) a comme résultat :
Devant ces images et le contexte, la patiente a bénéficié immédiatement (à l’admission) d’un test RT-PCR (reverse transcriptase chain reaction) réalisée par écouvillonnage oropharingien qui est revenue négative
Et L’Echographie cardiaque trouve une dilatation du ventricule droit et une hypertension artérielle pulmonaire à 50 mm Hg
Pour le traitement durant son séjour hospitalier : elle a bénéficié en dehors de l’oxygénothérapie à haute concentration (12 litres/min), d’un apport de soluté isotonique de serum salé (1500 ml/24h) ; de l’énoxaparine à dose curative (soit 200UI/Kg /J repartis en 2 injections S/C) Methyl - prednisolone 1 mg/kg en 2 prises administrés en IV et cela pendant 5 jours. Elle a reçu de l’azythromicine per os 500mgx2/j.
Après 5 jours, l’évolution était marquée au plan respiratoire par une amélioration avec une baisse de la fréquence respiratoire et des besoins en oxygène, au plan hémodynamique par une stabilité et au plan biologique, par la disparition de l’hyperleucocytose et la baisse remarquable des CRP. Elle est mise sortante sous anticoagulant : rivaroxaban 15 mgx2/j pendant 15 jours puis 20 mg/j et une lettre adressée à la consultation gynécologique en vue de revoir la méthode contraceptive.
Discussion
Vu le contexte de pandémie à corona virus, même en absence de symptomatologie de précession de l’évènement. Nous avons considéré la COVID-19 devant la fièvre, un syndrome inflammatoire biologique ; des images caractéristiques de pneumonie COVID-19 ; toute fois la patiente n’avait pas symptômes d’appel au préalable et la RT-PCR réalisée est revenue négative. Cela explique la non obtention du transfert de la patiente au service de prise en charge COVID-19. A postériori nous avons pu confirmer l’infection à SRAS-CoV-2 par le test sérologique d’IgG par ELISA montrant une réaction positive (forte réactivité avec l’antigène du SRAS-Cov2).
Les formes asymptomatiques et/ou présymptomatiques de la COVID-19[5] varient selon les études de 6, 4 à 12,6%. Notre patiente jusqu’à la survenue de sa détresse respiratoire objet de sa consultation à nos urgences pourrait être considéré comme une forme présymptomatique. Toute fois le test RT PCR pratiqué par voie oropharyngée est revenu négatif : en sachant que cette méthode peut ne pas déceler jusqu’à 40% des cas [6]. De plus certain cas cliniques décrie de thrombose sur COVID-19 démontrent qu’elles peuvent être des manifestations tardives de l’infection resté inapparente avec une RT-PCR négative mais le présence d’anticorps anti SRAS-CoV2 [7,8,9]. Cependant il est possible que ce soit l’événement thromboembolique qui permette la découverte de l’infection à SRAS CoV2 [9].
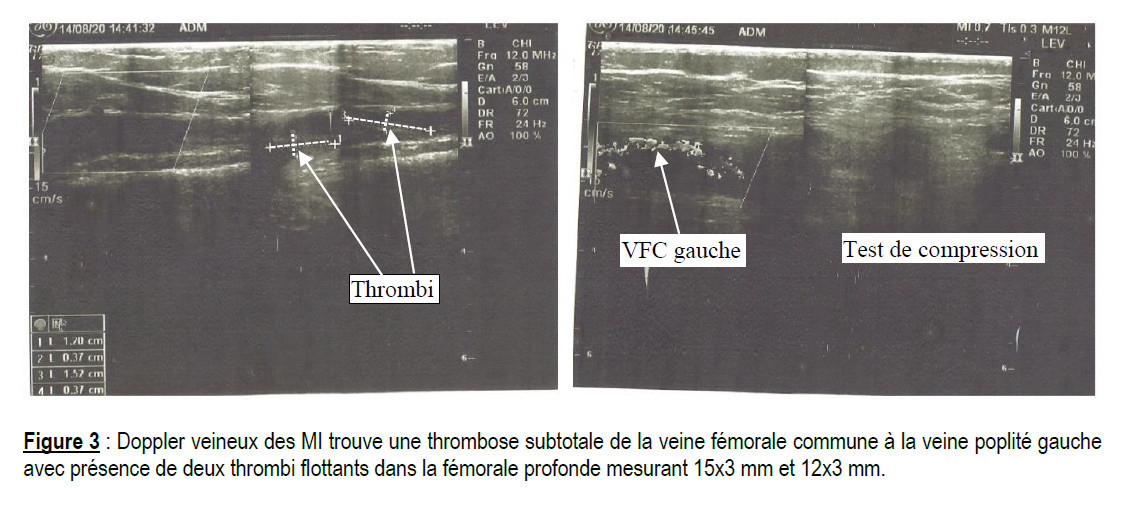
Les complications respiratoires et cardio-vasculaires sont des alternatives diagnostiques potentiellement mortelles chez les patients atteints de COVID-19[10]. Ces derniers présentent souvent des symptômes respiratoires se chevauchant largement avec la présentation clinique d'une EP aiguë. Il est donc important de savoir évoquer le diagnostic d'EP aiguë chez un patient atteint de COVID-19 devant toute détresse respiratoire d’aggravation brutale, l’apparition de signes évocateurs ou en cas de signes de thrombose veineuse profonde [11].Toute fois nous n’avions pas trouvé de signes cliniques en faveur d’une thrombo-phlébite à l’examen clinique (pas d’œdèmes aux membres inférieurs, pas d’induration sur un trajet veineux aux membre inférieurs et la dorsiflexion de la plante des pieds à la recherche de signe de Homans était négatif). Une revue de la littérature montre que la plupart des auteurs ont également fait le même constat chez les cas de thrombose veineuse des membres inférieurs sur COVID-19 [12]. En revanche le Doppler veineux des membres inférieurs a objectivé une thrombose subtotale de la veine fémorale commune à la veine poplitée gauche avec présence de deux thrombi flottants dans la fémorale profonde. Le critère diagnostic de la thrombose veineuse profonde est la compressibilité incomplète de la veine, ce qui indique la présence d'un caillot [13] ; nous avons tenu à reproduire cette technique (figure3)
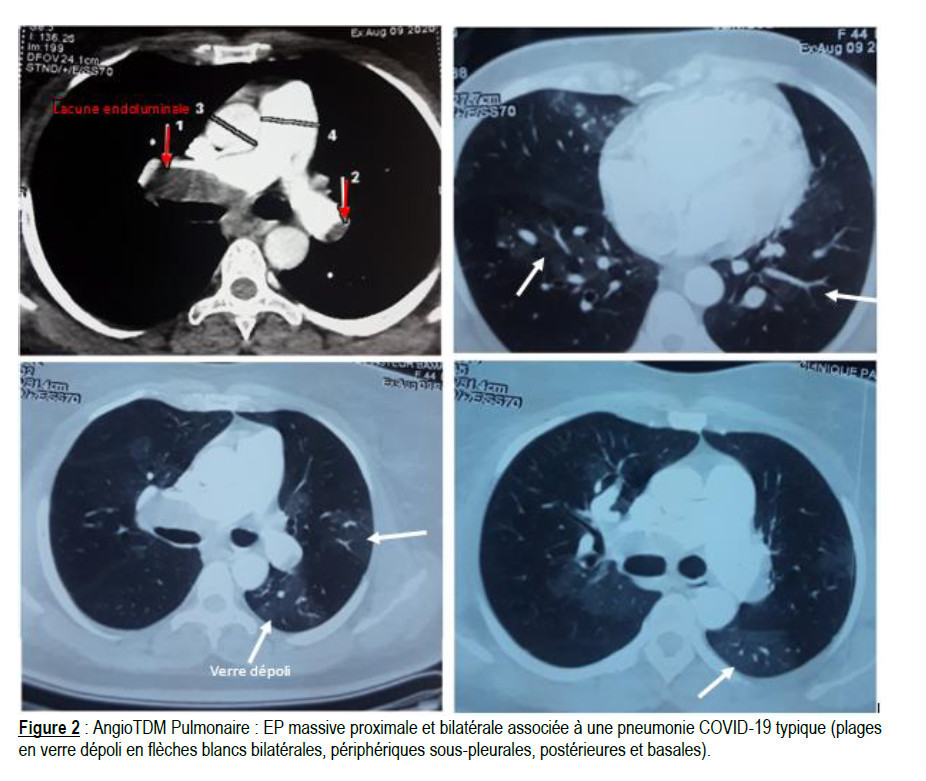
Le dosage des D-dimères [14] chez les patients atteints de COVID-19 est toujours conseillé dans la mesure où ce sont des marqueurs pronostiques, significativement augmentés chez les patients développant une forme sévère de Covid-19 nécessitant l’hospitalisation en réanimation ou entraînant le décès [15]. Ce dosage s’imposait à nous en urgence et va nous révéler un taux supérieur à 9 fois la normale. La combinaison de la symptomatologie et des résultats des examens (cliniques, biochimiques, biomarqueurs figure1) y compris les facteurs prédisposants chez notre patiente (obésité, COP) nous a conduit à la réalisation de l’angio TDM pulmonaire (figure2). Dans les recommandations, l'angio TDM pulmonaire multi-barrette est la méthode de choix pour l'imagerie pulmonaire vasculaire chez les patients suspectés d'EP. Il permet une visualisation adéquate des artères pulmonaires jusqu'au niveau sous-segmentaire [16]. Par ailleurs la TDM pulmonaire nous a permis de faire le diagnostic d’association à la pneumonie COVID typique (figure 2) (plages de verre dépoli bilatérales, périphériques sous-pleurales, postérieures et basales).
Conclusion : Notre observation est la preuve que la maladie à corona virus est polymorphe et multi systémique. Les ETEV sont de primun movens ; bien que sous-jacent évoluait une pneumonie COVID typique au stade asymptomatique à présymptomatique. Le défi que cela pose est à la fois, le mode opératoire quant au diagnostic et à la prise en charge. D’où la nécessité d’une équipe multidisciplinaire collaborative.
Conflit d’intérêt : Le Auteurs déclarent n’avoir aucun conflit d’intérêt en lien à cette publication.
Remerciement : A travers ce récit nous rendons hommage à la patiente qui est par la suite décédée quelques 3 mois après son exéat de l’hôpital alors qu’elle était en plein activité, mort subite ? Elle avait donné tous son consentement pour la divulgation de son cas.
Nos remerciements vont à l’endroit de tout le personnel des services de Cardiologie, de Maladies infectieuses et Tropicales et de l’imagerie médicale du CHU Point G.
Enfin nous remercions les collaborateurs de l’UCRC ‘’University Center for Clinical Research Center’’ pour avoir rendu possible de façon rétrospective le test sérologique IgG du SRAS-CoV-2 chez la patiente.
- Bonny V et al. COVID-19 : physiopathologie d’une maladie à plusieurs visages / La Revue de médecine interne 41 (2020) 375–389].
- Gupta A, Madhavan MV, Sehgal K, Nair N, Mahajan S, Sehrawat TS, et al. Extra-pulmonary manifestations of COVID-19. Nat Med 2020;26:1017–32]
- Bikdeli B, Madhavan MV, Jimenez D, Chuich T, Dreyfus I, Driggin E, et al. COVID-19 and thrombotic or thromboembolic disease: implications for prevention, antithrombotic therapy, and follow-up. J Am Coll Cardiol 2020;75:2950–73.
- Klok FA, Kruip MJHA, van der Meer NJM, Arbous MS, Gommers DAMPJ, Kant KM, et al. Incidence of thrombotic complications in critically ill ICU patients with COVID-19. Thromb Res 2020;191:145–7.
- Wei, W.E., Li, Z., Chiew, C.J., Yong, S.E., Toh, M.P. and Lee, V.J., 2020. Presymptomatic Transmission of SARS-CoV-2—Singapore, January 23–March 16, 2020. Morbidity and Mortality Weekly Report, 69(14), p. 411
- Xie X, Zhong Z, Zhao W et al. Chest CT for Typical 2019-nCoV Pneumonia: Relationship to Negative RT-PCR Testing. Radiology. 2020;200343.
- Schweblin C, Hachulla AL, Roffi M, Glauser F. Delayed manifestation of COVID-19 presenting as lower extremity multilevel arterial thrombosis: a case report. Eur Heart J Case Rep. 2020 Nov 19;4(6):1-4. doi: 10.1093/ehjcr/ytaa371. PMID: 33437919; PMCID: PMC7717202.
- Veyre F, Poulain-Veyre C, Esparcieux A, Monsarrat N, Aouifi A, Lapeze J, Chatelard P. Femoral Arterial Thrombosis in a Young Adult after Non severe COVID-19. Ann Vasc Surg. 2020 Nov;69:85-88. doi: 10.1016/j.avsg.2020.07.013. Epub 2020 Jul 28. PMID: 32736027; PMCID: PMC7386281.
- Santosa YP, Yuwono A. Two Different Clinical Presentations of Acute Limb Ischemia Caused by Acute Thrombotic Events in COVID-19. Cureus. 2021 Sep 12;13(9):e17916. doi: 10.7759/cureus.17916. PMID: 34660110; PMCID: PMC8511142.
- Long B, Brady WJ, Koyfman A, Gottlieb M. Cardiovascular complications in COVID-19. Am J Emerg Med 2020;38:1504–7
- Guan WJ, Ni ZY, Hu Y, Liang WH, Ou CQ, et al: China Medical Treatment Expert Group for C. Clinical Characteristics of Coronavirus Disease 2019 in China. N Engl J Med 2020.
- Mazzaccaro D, Giannetta M, Fancoli F, Milani V, Modafferi A, et al : COVID and venous thrombosis: systematic review of literature. J Cardiovasc Surg (Torino). 2021 Sep 14. doi: 10.23736/S0021-9509.21.12022-1. Epub ahead of print. PMID: 34520137.
- Da Costa Rodrigues J, Alzuphar S, Combescure C, Le Gal G, Perrier A. Diagnostic characteristics of lower limb venous compression ultrasonography in suspected pulmonary embolism: a meta-analysis. J Thromb Haemost 2016;14:1765_1772
- Kearon C, de Wit K, Parpia S, Schulman S, Afilalo M, Hirsch A, Spencer FA, Sharma S, D'Aragon F, Deshaies JF, Le Gal G, Lazo-Langner A, Wu C, Rudd-Scott L, Bates SM, Julian JA, Investigators PES. Diagnosis of Pulmonary Embolism with d-Dimer Adjusted to Clinical Probability. N Engl J Med 2019;381(22):2125-2134.
- Marchandot B, Trimaille A, Curtiaud A, Carmona A, Matsushita K, SatoC, et al. Staging severity of COVID-19 according to hemostatic abnormalities (CAHA Score). Thromb Haemost 2020:8–11, http://dx.doi.org/10.1055/s-0040-1715836.
- Konstantinides SV, Meyer G, Becattini C, et al ESC Scientific Document Group. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603. doi: 10.1093/eurheartj/ehz405. PMID: 31504429